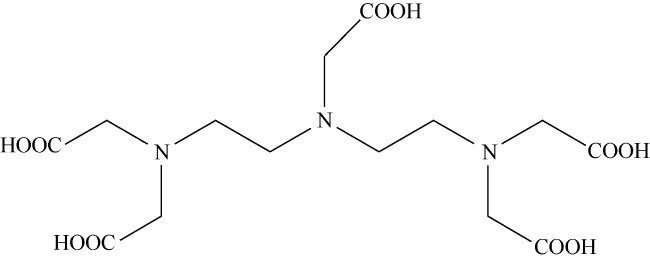
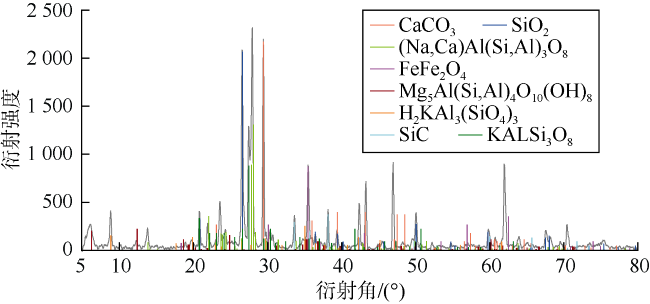
0 引言
1 实验介绍
1.1 实验材料
表1 盐水溶液离子组成 |
| 溶液名称 | 离子质量浓度/(mg·L−1) | 离子强度/(mol·L−1) | ||||||
|---|---|---|---|---|---|---|---|---|
| Na+ | Cl− | K+ | HCO3− | Mg2+ | Ca2+ | SO42− | ||
| SW | 12 649 | 23 287 | 459 | 92 | 1 641 | 499 | 3 069 | 0.83 |
| LSW(0.1 SW) | 1 264 | 2 328 | 45 | 9 | 164 | 49 | 306 | 0.83 |
| SW(1Ca2++0Mg2++0SO42−) | 18 384 | 29 607 | 459 | 92 | 0 | 499 | 0 | 0.83 |
| SW(3Ca2++0Mg2++0SO42−) | 17 234 | 29 604 | 459 | 92 | 0 | 1 499 | 0 | 0.83 |
| SW(0Ca2++1Mg2++0SO42−) | 15 856 | 29 615 | 459 | 92 | 1 641 | 0 | 0 | 0.83 |
| SW(0Ca2++3Mg2++0SO42−) | 9 651 | 29 625 | 459 | 92 | 4 925 | 0 | 0 | 0.83 |
| SW(0Ca2++0Mg2++1SO42−) | 17 464 | 25 039 | 459 | 92 | 0 | 0 | 3 069 | 0.83 |
| SW(0Ca2++0Mg2++3SO42−) | 14 477 | 15 898 | 459 | 92 | 0 | 0 | 9 207 | 0.83 |
注:SW代表海水,LSW代表低矿化度水,括号里的数字是海水中相应离子浓度的倍数 |
1.2 实验方法
1.2.1 接触角测量
1.2.2 Zeta电位的测量
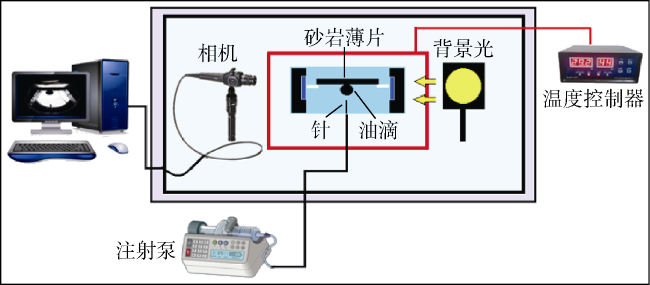
1.2.3 自发渗吸实验
表3 自发渗吸实验砂岩岩心物性参数 |
| 岩心编号 | 长度/m | 直径/cm | 孔隙度/% | 渗透率/10−3 μm2 |
|---|---|---|---|---|
| 1 | 7.5 | 3.8 | 18.5 | 74.6 |
| 2 | 7.5 | 3.8 | 18.2 | 73.3 |
| 3 | 7.2 | 3.8 | 19.3 | 75.6 |
| 4 | 7.3 | 3.8 | 18.8 | 76.9 |
2 结果与讨论
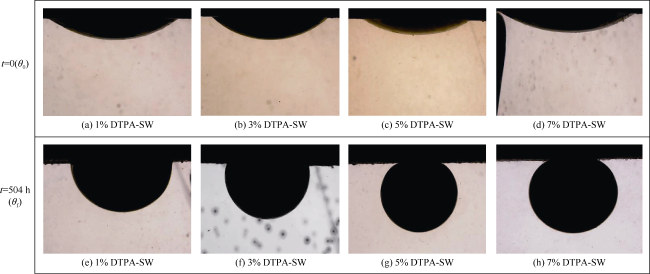
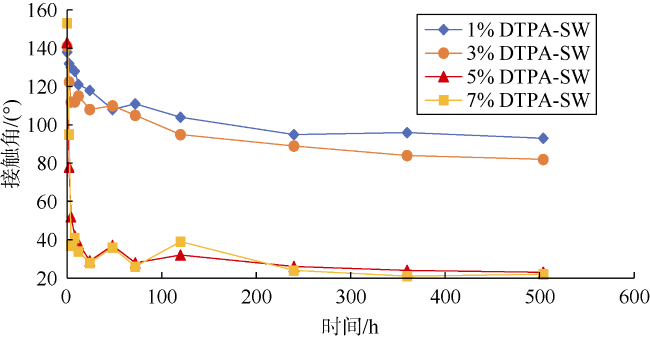
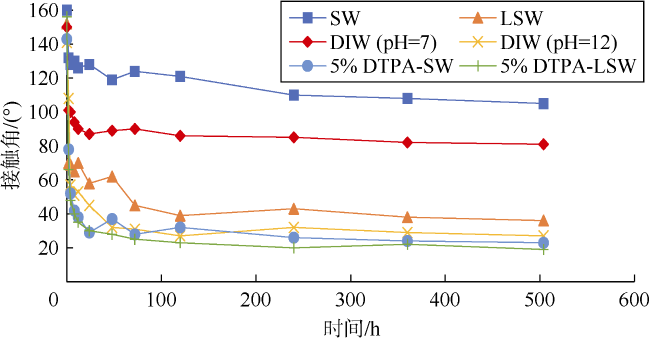
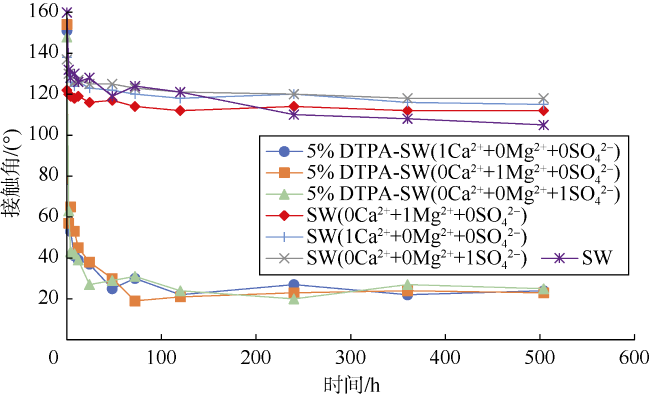
2.1 润湿性改变
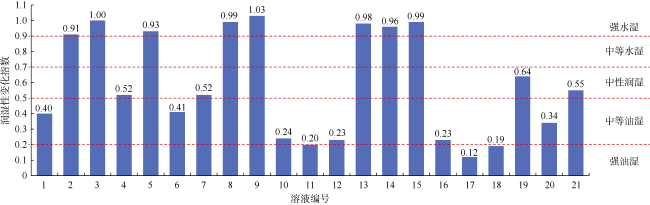
表4 不同溶液的润湿性变化指数 |
| 溶液 编号 | 溶液 | θi/ (°) | θ0/ (°) | θf/ (°) | 润湿性 变化指数 |
|---|---|---|---|---|---|
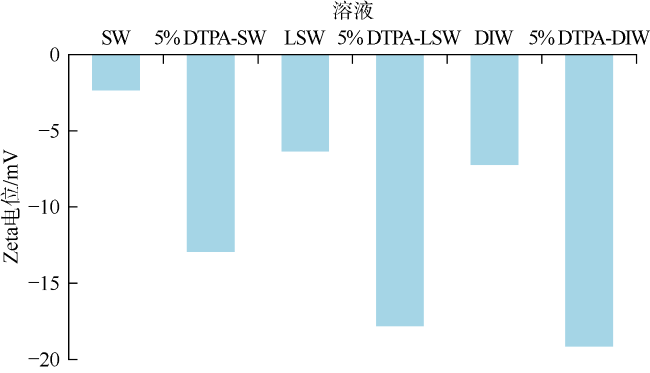
| 1 | SW | 28 | 160 | 105 | 0.40 |
| 2 | LSW | 24 | 152 | 36 | 0.91 |
| 3 | 5% DTPA-LSW | 21 | 156 | 19 | 1.00 |
| 4 | 去离子水(pH=7) | 21 | 150 | 81 | 0.52 |
| 5 | 去离子水(pH=12) | 18 | 141 | 27 | 0.93 |
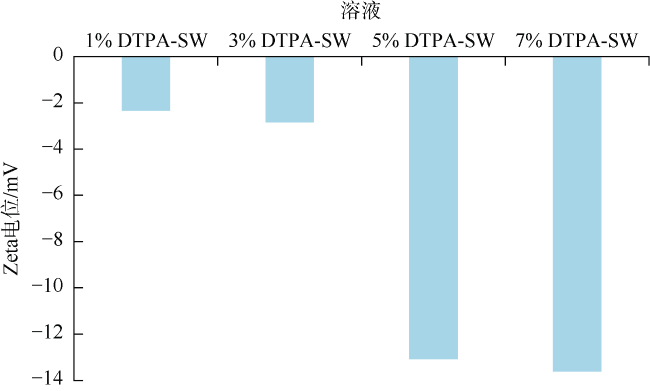
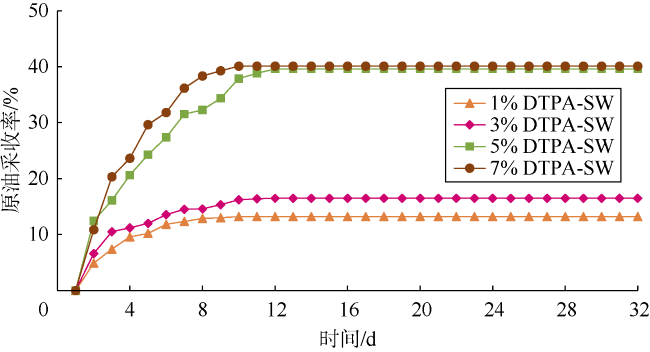
| 6 | 1% DTPA-SW | 30 | 138 | 93 | 0.41 |
| 7 | 3% DTPA-SW | 28 | 141 | 82 | 0.52 |
| 8 | 5% DTPA-SW | 22 | 143 | 23 | 0.99 |
| 9 | 7% DTPA-SW | 27 | 153 | 22 | 1.03 |
| 10 | SW(1Ca2++0Mg2++0SO42-) | 23 | 144 | 115 | 0.24 |
| 11 | SW(0Ca2++1Mg2++0SO42-) | 28 | 133 | 112 | 0.20 |
| 12 | SW(0Ca2++0Mg2++1SO42-) | 28 | 145 | 118 | 0.23 |
| 13 | 5% DTPA-SW(1Ca2++0Mg2++0SO42-) | 21 | 151 | 24 | 0.98 |
| 14 | 5% DTPA-SW(0Ca2++1Mg2++0SO42-) | 18 | 154 | 23 | 0.96 |
| 15 | 5% DTPA-SW(0Ca2++0Mg2++1SO42-) | 24 | 148 | 25 | 0.99 |
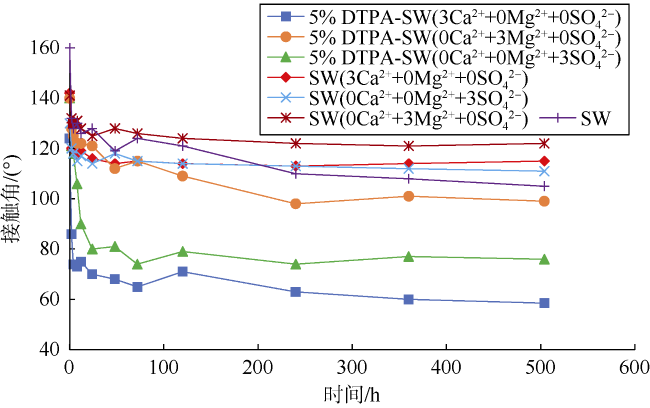
| 16 | SW(3Ca2++0Mg2++0SO42-) | 25 | 142 | 115 | 0.23 |
| 17 | SW(0Ca2++3Mg2++0SO42-) | 31 | 135 | 122 | 0.12 |
| 18 | SW(0Ca2++0Mg2++3SO42-) | 30 | 130 | 111 | 0.19 |
| 19 | 5% DTPA-SW(3Ca2++0Mg2++0SO42-) | 22 | 124 | 58 | 0.64 |
| 20 | 5% DTPA-SW(0Ca2++3Mg2++0SO42-) | 21 | 140 | 99 | 0.34 |
| 21 | 5% DTPA-SW(0Ca2++0Mg2++3SO42-) | 24 | 140 | 76 | 0.55 |
注:除溶液5外,其他溶液pH值均约为7 |