第一作者简介:林梅钦(1965-),男,福建连江人,硕士,中国石油大学(北京)提高采收率研究院副教授,主要从事胶体与界面化学及提高石油采收率方面的教学与研究工作。地址:北京市昌平区水库路18号,中国石油大学(北京)提高采收率研究院,邮政编码:102249。E-mail: linmq@cup.edu.cn
基于岩石表面基团与有机物分子间的黏附模型,分析油藏岩石表面的化学基团与原油中不同组分之间的微观作用力以及岩石表面和原油-盐水界面处双电层之间的相互作用,研究盐水中H+、OH-和无机盐离子对岩石表面润湿性的调节能力及其微观机制,并建立了油藏润湿性调节的新方法。原油中有机物质与岩石表面基团之间存在范德华力、氢键、库仑力和表面力相互作用,改变这些相互作用力,利用盐水调节岩石表面润湿性的机理包括:化学基团转化、界面电势改变、注入水pH值改变、多组分离子交换及盐溶/盐析效应。对砂岩油藏,随着盐水中阳离子价态、盐水浓度降低或盐水pH值(对矿化度影响不大)增加,原油与岩石表面间相互作用变弱,岩石表面亲水性增强;对碳酸盐岩油藏,高矿化度CaSO4、MgSO4盐水有利于增强油藏岩石表面亲水性。因此通过调节注入水的离子组成可调控油藏岩石表面亲水性,提高原油采收率。
Based on adhesion models between rock surface groups and organic molecules, the interactions between the chemical groups on the rock surface and the components of crude oil and the interactions of the electrical double layers at the rock surface and oil-water interface were analyzed to investigate the abilities and microscopic mechanisms of wettability control by H+, OH- and inorganic salt ions in brine, and a new method of wettability control for reservoir rocks was built. The results show that the interaction forces between rock surface groups and oil molecules are van der Waals forces, Coulomb forces, hydrogen bonds, and surface forces. By changing these forces, the control mechanisms of surface wettability of reservoir rocks by brine are: transformation of chemical groups, change of interfacial potential, pH variation of injected water, multicomponent ionic exchange, and salting-in or salting-out effect. For sandstone reservoirs, with the decrease of concentration and valence state of positive ions in brine or the increase of pH (increasing pH has a negligible impact on the brine salinity), the interaction between rock surface and oil becomes weak, thus resulting in increase of water wettability of rock surface. For carbonate reservoirs, CaSO4 or MgSO4brine with high concentration is beneficial to increase water wettability of rock surface. Therefore, it is feasible to control rock wettability and improve oil recovery by adjusting the ion components of injected water.
润湿性为储集层物性的一个基本特性参数, 它是影响毛细管力、微观波及体积和残余油饱和度的重要因素。因此, 合理调节岩石润湿性对油藏有效开发十分重要。目前润湿性调节化学剂主要是表面活性剂[1, 2]。由于表面活性剂特殊的分子结构, 导致它在使用时存在很多缺点:①价格较昂贵; ②对硬水很敏感; ③耐温性差; ④在地层中易发生吸附损失, 给环境造成不利影响; ⑤对其结构、浓度和用量要求苛刻。因此设计一种高效、廉价易得、耐温耐盐及绿色环保的润湿性调节剂意义重大。
大量室内和矿场试验证明盐水能有效调节岩石表面润湿性。Nasralla等[3]通过接触角测定实验发现, 减小注入水中盐离子浓度或者增大其pH值时, 岩石-盐水-原油体系中水在岩石表面的接触角明显减小, 岩石表面由中性转变为亲水性。HUA等[4]通过岩心在不同盐水中的渗吸实验发现, 当盐水中Ca2+浓度增加, 盐水的渗吸速率显著降低, 岩石表面亲水性变弱; 减小盐水中Ca2+浓度或盐水矿化度, 盐水渗吸易发生, 岩石表面亲水性增强。Rezaeidoust等[5]发现Ca2+、SO42-和Mg2+、SO42-组合能使碳酸盐岩表面亲水性增强, 从而增强碳酸盐岩储集层的渗吸能力, 有利于提高此类储集层采收率。Vledder等[6]分析裸眼井测井数据, 从矿场试验上证明了降低注入水矿化度可使油藏从混合润湿或油湿变为水湿。通过调节注入水中离子组成来调控岩石润湿性从而提高原油采收率技术在国外引起了广泛重视, 低矿化度水驱技术[7]在Alaskan油田[8]、Snorre油田[9, 10]、中东油田[6, 11]等已得到应用并取得了显著效果。
本文根据岩石-盐水-原油间的8种黏附模型对岩石表面基团与有机物之间的相互作用力进行分析, 探讨盐水调节岩石润湿性的微观机理, 从而建立用盐水调控岩石润湿性的方法, 对于科学制定注入水的离子组分的标准、正确认识岩石润湿特性以及探索提高采收率方法等提供借鉴。
砂岩储集层或碳酸盐岩储集层主要由不同晶体结构和性质的硅酸盐矿物和碳酸盐矿物组成, 这些岩石矿物主要成分包括石英、长石、方解石、白云石及黏土矿物(如绿泥石、伊蒙混层矿物、高岭石和伊利石)。从微观角度出发, 这些岩石表面分布不同种类和数密度的化学基团。例如石英(SiO2)属于原子晶体, 其表面主要由3种不同电性的硅醇基团(≡ Si— OH, ≡ Si— OH2+, ≡ Si— O-)组成[12]。长石一般化学式为M[T4O8](M代表K、Na、Ca元素, T代表Si、Al元素), 是一类架状基型的硅酸盐, 其表面基团主要包括不同电性的硅醇基团或者铝醇基团(≡ Al— OH, ≡ Al— OH2+, ≡ Al— O-)[13]。高岭石Al4[Si4O10](OH)8、蒙脱石(Al, Mg)2[Si4O10](OH)2· nH2O等黏土矿物都属于层状结构的硅酸盐, 它们的表面化学基团也主要是硅醇基团或者铝醇基团[14, 15, 16]。方解石CaCO3、白云石CaMg(CO3)2属于岛状基型的碳酸盐, 为离子晶体, 其表面阳离子主要是≡ CO3Ca+, 阴离子主要为≡ CaCO3-[17]。岩石表面基团在油藏条件下可互相转化, 以硅酸盐为例:
$\equiv \text{T}--\text{OH}$$^{\underrightarrow{\text{$K^{-}_{d}$}}}_{\overleftarrow{\text{ }}}$$\equiv \text{T}--{{\text{O}}^{-}}+{{\text{H}}^{+}}$
$\equiv\text{T}--\text{O}{{\text{H}}_{2}}^{+}$$^{\underrightarrow{\text{$K^{-}_{d}$}}}_{\overleftarrow{\text{ }}}$$\equiv \text{T}--\text{OH}+{{\text{H}}^{+}}$
其中, 由表面化学基团的解离方程可知砂岩表面带电的基团(≡ T— O– 、≡ T— OH2+)密度由溶液中定势离子H+浓度决定[18, 19]:
${{\sigma }^{-}}={{f}^{-}}{{\sigma }_{0}}=\frac{K_{\text{d}}^{-}}{K_{\text{d}}^{-}+{{[{{\text{H}}^{+}}]}_{\infty }}{{\text{e}}^{-e{{\varphi }_{0}}/k{{T}_{{}}}}}}{{\sigma }_{0}}$ (1)
${{\sigma }^{+}}=\left( 1-{{f}^{+}} \right){{\sigma }_{0}}=\frac{{{[{{\text{H}}^{+}}]}_{\infty }}{{\text{e}}^{-e{{\varphi }_{0}}/kT}}}{K_{\text{d}}^{+}+{{[{{\text{H}}^{+}}]}_{\infty }}{{\text{e}}^{-e{{\varphi }_{0}}/kT}}}{{\sigma }_{0}}$ (2)
岩石表面化学基团具有不同的电量和极性, 与液体分子间具有不同的相互作用势能, 从而导致岩石表面润湿程度不同。很多研究者测试了不同矿物的亲水性[20], 发现石英、长石类矿物亲水性较强, 而碳酸盐矿物的亲水性较弱。由于黏土矿物中硅氧四面体晶片层、铝氧八面体晶片层和端面上的结构电荷不平衡, 黏土矿物表面带有负电, 因此黏土矿物通常被视为阳离子交换材料。不同黏土矿物的晶体结构和结构单元差异较大, 导致它们的阳离子交换能力不同, 蒙脱石的阳离子交换能力最强, 其次是伊利石和绿泥石, 最弱的是高岭石[21]。黏土矿物的阳离子交换能力决定了岩石表面对其周围水溶液中阳离子和原油中极性组分的吸附能力, 进而影响了岩石的润湿性。Dubey等[22]曾认为油藏条件下石英表面保持完全亲水。然而孔隙壁上通常会黏附大量带电的黏土矿物, 黏土矿物对岩石的润湿性存在较大的影响, 例如蒙脱石吸水能力较强, 故它的存在会增强岩石的亲水性, 而含有铁的黏土矿物, 如鲕状绿泥石(Fe3Al2Si2O10· 3H2O), 因为铁具有从原油中吸附表面活性物质的能力, 它的存在会使岩石表面局部变为亲油[23]。
石油是非常复杂的混合物, 其中的碳和氢含量可达95%~99%, 杂原子(主要为硫、氧、氮元素)含量一般为1%~5%。虽然硫、氧、氮元素含量很低, 但这些元素以碳氢化合物的衍生物形式存在, 例如硫在原油中主要以硫醇、硫醚、二硫化物、噻吩及其同系物形态存在; 含氧化合物包括环烷酸、脂肪酸、酚类、酸酐、醚类、酯类、酮类、酰胺及其他含氧化合物, 常呈酸性或中性; 含氮化合物主要包括吡啶、喹啉、胺、咔唑、吡咯及它们的衍生物, 一般呈碱性或中性[24]。所以含硫、氧、氮元素的化合物在石油中的含量相对大得多。这些非烃组分是原油中的极性成分, 主要分布在胶质、沥青质中, 它们具有较强的界面活性, 能够改变矿物表面的润湿状态[25]。含硫、氧、氮元素的分子一端为极性基团, 这些极性基团通过库仑力或氢键作用吸附在矿物表面[18], 另一端烃基则暴露在外面, 从而导致岩石表面亲油性增强。在不同pH值条件下, 非烃组分中的极性基团会发生质子化或去质子化过程, 从而改变了非烃组分的带电量, Harding和Healy[26]建立理论模型, 解释了盐水pH值对原油中有机酸、有机碱解离程度及原油-盐水界面电势的影响规律:
$\text{AH}$$^{\underrightarrow{\text{ }}}_{\overleftarrow{\text{ }}}$${{\text{A}}^{-}}+{{\text{H}}^{+}}$
$\text{B}+{{\text{H}}^{+}}$$^{\underrightarrow{\text{ }}}_{\overleftarrow{\text{ }}}$$\text{B}{{\text{H}}^{+}}$
原油中有机酸和有机碱具有不同的荷电机理, 它们与岩石表面各基团之间具有不同的相互作用力。在无水的条件下, 表面带负电基团的石英或硅酸盐矿物更倾向于吸附有机碱, 包括脂肪胺[27]、吡啶[28, 29]等; 而表面带有正电基团的碳酸盐矿物更倾向于吸附有机酸, 包括环烷酸[30]、脂肪酸[31]。此条件下有机酸或有机碱是通过酸碱反应吸附在岩石表面。当有水存在时, 有机酸、有机碱可以通过离子架桥分别吸附在砂岩或碳酸盐岩表面[8, 32, 33]。
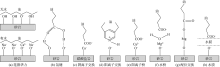
从微观角度出发, 原油中含有各种极性或非极性的分子链, 这些分子链与岩石表面各类带电或中性基团之间存在相互作用力, 可归纳为图1所示的8种[8, 32, 34, 35]。这些力包括范德华力、氢键、库仑力和表面力。不同有机物与不同岩石表面间存在不同的吸附机理。原油中的烃类化合物, 主要依靠范德华力吸附在岩石表面。岩石表面分布各种带电或中性的基团, 这些基团与烃类化合物间的作用力属于电荷和诱导偶极间的诱导力。这种相互作用势能可表示为[18]:
${{E}_{1}}=-\frac{Q_{1}^{2}\alpha }{2{{(4\text{ }\!\!\pi\!\!\text{ }{{\varepsilon }_{0}})}^{2}}r_{1}^{4}}$ (3)
由(3)式可知, 原油中的烃类化合物与岩石表面间的相互作用势能与岩石表面带电粒子分布相关。岩石表面带电粒子由岩石表面带电的基团和紧密吸附在岩石表面的反离子组成, 由于岩石表面带电基团受水相pH值调控, 反离子由注入水中无机盐离子组成, 所以烃类化合物与岩石表面间的相互作用势能受注入水中的H+、OH-和无机盐离子组成强烈影响。
原油中的氨基、羰基、羧基及酚类化合物中的羟基易与岩石表面不同电性的硅醇基团或者铝醇基团以氢键结合(见图1b)。这种氢键作用属于电荷和永久偶极间的库仑力[18]:
${{E}_{2}}=-\frac{{{Q}_{1}}\mu \text{cos}\theta }{4\text{ }\!\!\pi\!\!\text{ }{{\varepsilon }_{0}}r_{2}^{2}}$ (4)
不同电性的表面基团具有不同的极性, 因而与原油中活性组分之间形成的氢键强弱也就不同。
原油中的羧酸盐会取代吸附在碳酸盐岩表面的阴离子而发生阴离子交换吸附, 即羧酸盐将直接吸附在碳酸盐岩表面带正电的基团(≡ CO3Ca+)上(见图1c)。然而原油中的季铵盐和含氮的杂环化合物会取代吸附在砂岩表面的阳离子而发生阳离子交换吸附, 即季铵盐和含氮的杂环化合物将直接吸附在砂岩表面负电性硅醇基团(≡ SiO-)上(见图1d)。可交换阳离子会在原油中的氨基、羰基、羧基及醇羟基与岩石表面之间形成桥梁作用(见图1e)。当岩石表面可交换的阳离子溶剂化能力很强时, 如Mg2+, 图1e中的阳离子桥会转化为水桥(见图1f)。这4类吸附模型(见图1c— 图1f)中, 原油中有机物分子上的带电基团与岩石表面的带电基团通过电荷与电荷间的库仑力相互作用, 这种相互作用势能可以表示为[18]:
${{E}_{3}}=-\frac{{{Q}_{1}}{{Q}_{2}}}{4\text{ }\!\!\pi\!\!\text{ }{{\varepsilon }_{0}}{{r}_{3}}}$ (5)
由(5)式可知, 当原油中的极性组分通过离子交换吸附在岩石表面时, 它们之间的相互作用势能与带电基团的带电量和带电的正负性相关。
在岩石表面多价阳离子和原油中的羧酸盐之间还可能直接形成配位键(见图1g), 该化学键比阳离子桥和阳离子交换键作用要强, 从而导致羧酸和二价金属离子能够一起从岩石表面脱离下来形成有机金属络合物(RCOOM+, M表示二价阳离子)。
如果形成油层前岩石表面是水湿的, 原油运移进入储集层后, 在原油与岩石之间会形成一层水膜(见图1h), 此时岩石表面与原油-盐水界面间的相互作用可以用表面力模型来描述[36, 37, 38]:
${{p}_{\text{c}}}=\Pi =$$\frac{2\varepsilon {{\varepsilon }_{0}}{{\kappa }^{2}}\left[ {{\varphi }_{1}}{{\varphi }_{2}}\left( {{\text{e}}^{\kappa h}}+{{\text{e}}^{-\kappa h}} \right)-\left( \varphi _{_{1}}^{2}+\varphi _{2}^{2} \right) \right]}{{{\left( {{\text{e}}^{\kappa h}}-{{\text{e}}^{-\kappa h}} \right)}^{2}}}-\frac{A}{6\text{ }\!\!\pi\!\!\text{ }{{h}^{3}}}+{{A}_{\text{s}}}{{\text{e}}^{-\frac{h}{{{h}_{\text{s}}}}}}$(6)
(6)式中Π 为单位膜面积上能量对膜厚度的偏微分, 为静电力、范德华力和结构力(也称溶剂化作用, 由水分子结构引起, 是距离小于1 nm的短程力)之和, Hamaker常数约为10-20J[36]。在Takahashi[37]研究工作中, 取As=1.5× 1010Pa, hs=0.05 nm。
油藏在原始条件下, 岩石-地层水-原油达到了受力平衡状态。注水开发时, 由于地层水与注入水中各种离子(H+、OH-和无机盐离子)含量不同, 会发生离子扩散现象, 引起地层水中各离子含量发生变化, 从而导致岩石-地层水-原油间的受力平衡遭到破坏, 岩石润湿性也随之发生改变。针对不同离子组成的盐水, 岩石(砂岩或碳酸盐岩)润湿性具体变化机理如下。
3.1.1 化学基团转化
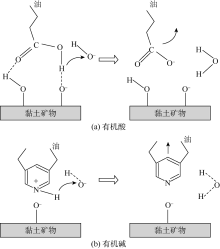
注入水的pH值会影响硅酸盐[39, 40]和碳酸盐矿物表面基因[17]及有机酸、有机碱[41]的质子化和去质子化过程, 从而控制了岩石表面的化学基团组成[38]、有机酸和有机碱中极性基团组成, 进而决定了岩石表面和原油-盐水界面处反离子的吸附量。岩石表面基团与原油中有机物之间存在范德华力、氢键、库仑力和表面力。由(3)— (6)式可知, 不同的基团与原油中有机物间的相互作用存在明显差异。例如随着注入水的pH值增大, 砂岩表面大量中性基团(≡ T— OH)转化为带负电的基团(≡ T— O-), 岩石表面带电基团(≡ T— O-)数量增多。同时原油中的有机酸和有机碱的质子化和去质子化过程受pH值控制, 注入水的pH值增大会引起酸碱质子转移反应。反应后有机酸和有机碱中的极性基团的带电量发生改变, 从而与岩石表面基团间的相互吸引作用变弱, 如图2a中有机酸与岩石表面间的氢键作用转化为静电排斥力; 图2b中有机碱与岩石表面间的较强库仑力作用转化为一种较弱的库仑力作用[21]。最终导致吸附在岩石矿物表面的有机酸和有机碱发生脱附作用, 岩石表面的亲水性从而增强。
有机酸和有机碱在黏土矿物表面的吸附或脱附过程对溶液pH值变化非常敏感, 反应方程式总结如
下[21]:
≡ R— RCOOH+OH- == ≡ R+RCOO-+H2O
≡ W— NHR3++OH- == ≡ W+R3N+H2O
Madsen和Ida[42]研究了羧酸物质在黏土矿物表面的吸附作用, 同样发现该吸附过程对溶液pH值非常敏感, 羧酸物质在黏土矿物表面的吸附量随溶液pH值增大而减小。
3.1.2 界面电势改变
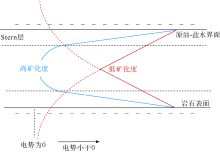
注入水的pH值会影响岩石表面化学基团组成、原油中有机物的极性基团组成及岩石-盐水界面和原油-盐水界面双电层中的电势分布(见图3), 从而影响了各界面处的电动电势。随着盐水pH值增大, 两界面处的电动电势都变得更负, 此时岩石-盐水界面与原油-盐水界面之间静电排斥力增大, 那么岩石表面的水膜将更加稳定, 岩石表面表现得更加亲水。Nasralla等[3]通过电动电势测定和接触角测试实验发现, 降低注入水pH值时, 岩石-盐水界面和原油-盐水界面处的电动电势将减小, 从而减弱了油与岩石表面之间的静电斥力, 导致岩石表面更加亲油。Takahashi[37]研究硅质页岩- NaBr盐水-原油间相互作用, 理论计算发现随着盐水pH值增加(pH< 4), 岩石与原油间的液膜分离压数值不断变小, 液膜变得不稳定。当溶液pH值继续增大(pH> 4)时, 岩石-盐水界面和原油-盐水界面处带有的负电荷同时增多, 两处的电动电势将增大, 导致岩石-盐水界面与原油-盐水界面间的静电排斥力增大, 即两界面中的液膜分离压变得更大, 液膜厚度变大。因此在适中的pH值(pH≈ 4)条件下, 岩石表面亲水性较弱, 当增大或减小注入水的pH值时, 岩石表面亲水性增强。
 | 图3 高、低pH值条件下原油-盐水界面和岩石表面 双电层Stern模型中的电势分布[33] |
3.2.1 注入水pH值发生改变
注入水中的H+会与吸附在岩石表面的Ca2+发生竞争吸附, 从而导致注入水的pH值发生改变, 进而影响了岩石表面的化学基团和有机物中极性基团的带电量和电性。Rezaeidoust等[5]研究表明, 低矿化度水驱时采出液pH值会出现增加。在油藏条件下, 黏土矿物表面最初会吸附地层水中高价阳离子(尤其是Ca2+)。在低矿化度水驱时, 由于注入水中离子浓度远远低于地层水, 原始条件下岩石-盐水相互作用的平衡状态被打破, 阳离子(尤其是Ca2+)将从岩石表面脱附下来, 此时岩石周围水分子电离出来的H+会吸附到岩石表面上, 导致岩石周围水溶液pH值局部增加, 此过程反应方程式如下[5, 21]:
≡ W— Ca2++H2O==≡ W— H++Ca2++OH-
3.2.2 扩散双电层厚度改变
带电的矿物表面或原油-盐水界面会吸引周围液体介质中的反离子, 这些反离子在两相界面呈扩散状态分布而形成扩散双电层, 其中扩散双电层厚度可表示为[18, 43]:
${{\kappa }^{-1}}=\sqrt{\frac{{{\varepsilon }_{0}}\varepsilon kT}{\sum\limits_{i}{{{c}_{i}}{{N}_{\text{A}}}{{e}^{2}}z_{i}^{2}}}}$ (7)
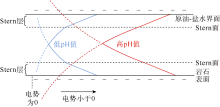
因此注入水中无机盐离子的浓度会影响岩石表面和原油-盐水界面处的扩散双电层厚度及双电层中电势分布情况(见图4), 从而影响了岩石-盐水界面和原油- 盐水界面处的电动电势。如前面所述, 改变电动电势将会引起岩石表面润湿性发生变化。Yukselen等[43]研究发现, 阳离子的水合半径和价态决定其降低岩石表面(或者原油-盐水界面)电动电势的能力。Yukselen等[43]研究结果表明, 0.01 mol/L不同阳离子溶液降低高岭土表面电动电势的能力排序为:Ca2+ > Mg2+ > Li+ > Na+。地层水中的多价金属离子(Ca2+、Mg2+)在带负电的油滴和黏土矿物间产生桥梁作用[32, 33, 44]。当注入水含盐量较高时, 大量的阳离子能够有效屏蔽油滴和黏土矿物表面的负电量, 导致两个带电界面上滑动面处的电动电势降低, 因此减弱了它们之间的静电排斥力。Nasralla等[3]通过电动电势测定和接触角测试实验发现, 当增加注入水中盐离子浓度, 岩石表面和原油-盐水界面处的电动电势将减小, 从而减弱了油与岩石表面之间的静电斥力, 导致岩石表面更加亲油。Hirasaki[36]研究发现, 随着电解质溶液中的无机盐浓度增大, 岩石表面液膜的分离压等温线上的峰值不断减小, 平衡液膜的厚度会减小, 亲水性减弱; 当盐浓度达到0.1 mol/L时, 该峰值接近于零; 当盐浓度进一步增大时, 该峰值小于零, 此时液膜的分离压由范德华力和结构力控制, 岩石表面液膜容易破裂, 岩石表面亲水性进一步减弱。
当注入水的矿化度下降时, 岩石表面与原油-盐水界面处的扩散双电层厚度变大, 同时岩石表面和原油-盐水界面处的电动电势将增大。这将导致黏土颗粒和油滴间的静电排斥力增大, 当排斥力大于阳离子桥梁产生的键合力时, 油滴将从岩石表面脱附下来, 岩石表面亲水性将增强[6]。但如果注入水的矿化度继续减小, 黏土矿物间的排斥力会超过其间的键合力, 黏土矿物将发生反絮凝作用, 造成储集层伤害。Suijkerbuijk等[45]发现当地层水矿化度很高(二价阳离子含量高)时, 高浓度NaCl溶液的自渗吸作用很有限, 可能相对地层水中二价阳离子而言, 水溶液中的置换离子Na+含量较少; 当稀释NaCl溶液时原油采收率得到显著提高, 该实验结果归因于岩石表面和原油-盐水界面处扩散双电层的扩张。
3.2.3 多组分离子交换
由于带电基团对反离子存在静电吸引力和范德华力作用, 所以在岩石表面形成了一个固定的反离子吸附层[38], 原油中的界面活性组分可以直接吸附或通过形成有机金属络合物吸附在岩石表面, 在低矿化度水驱过程中, 多组分阳离子交换过程将会发生, 简单的阳离子将会从岩石表面将原油中界面活性组分和有机金属络合物取代下来, 从而使岩石表面变得更加亲水。Lager等[32]对阿拉斯加北坡油田低矿化度水驱采出液进行分析得到:采出液中Mg2+浓度明显低于注入水和地层水中Mg2+的浓度, 说明Mg2+在岩石基质中会发生强烈吸附作用。Rueslatten等[46]指出, 当注入水中盐含量很高时, 原油会与黏土颗粒反应生成有机金属络合物(见图1g), 这将导致黏土矿物表面局部亲油。Lager等[32]研究发现低矿化度水驱能增加油藏岩石表面亲水性。因为地层水中一定含有二价阳离子, 吸附在黏土矿物表面的多价阳离子能够与原油中极性组分形成有机金属络合物, 该络合物能够提高油藏的亲油性[46]。同时部分极性有机组分会取代黏土矿物表面的最不稳定阳离子而直接吸附在其表面上(见图1d)。在低矿化度水驱过程中, 将会发生多组分阳离子交换, 简单的阳离子将会从黏土矿物表面将极性有机组分和有机金属络合物取代下来。极性组分的脱附过程将导致岩石表面亲水性增强和最终采收率提高。Suijkerbuijk等[45]、Lager等[8, 32]发现高浓度NaCl盐水驱能有效地提高原油采收率, 这是多组分离子交换的结果; 同时发现后续的低浓度NaCl盐水驱还能进一步提高原油采收率, 这可能是岩石表面扩散双电层扩张的贡献。当黏土矿物作为阳离子交换剂时, 多组分阳离子交换是指吸附在黏土矿物表面的阳离子可能被其他阳离子取代, 常见阳离子置换顺序为:Li+< Na+< K+< Mg2+< Ca2+< Ba2+< Al3+< Fe3+< H+。对于碳酸盐岩储集层, 岩石表面的化学基团与砂岩存在明显差异。原油中极性成分与碳酸盐岩表面基团的化学成键机理也与砂岩明显不同。Rezaeidoust等[5]发现Ca2+、SO42-和Mg2+、SO42-能使碳酸盐岩表面亲水性增强, 从而增强碳酸盐岩储集层的自渗吸能力, 有利于提高此类储集层采收率。以Ca2+、SO42-作为改性剂为例说明碳酸盐岩表面润湿性改变机理。首先SO42-会优先吸附在带正电的碳酸盐岩表面, 中和其表面的部分正电荷, 从而Ca2+与碳酸盐岩表面间的排斥力减弱, 此时更多的Ca2+会吸附到岩石表面, 与羧酸物质反应而将它从碳酸盐岩表面取代下来, 此改性机理见图5a。改性过程的反应方程式为:
RCOO– — Ca— CaCO3+ Ca2++SO42– ==
RCOO— Ca++ Ca— CaCO3+ SO42–
在此过程中, SO42-起到了类似催化剂的作用, 促进Ca2+在岩石表面富集。Rezaeidoust等[5]发现随着温度增加, Ca2+在碳酸盐岩表面吸附量增加, 这是由于高温(130 ℃)条件下在SO42-周围的水分子结构会遭到破坏, SO42-的反应活性会得到提高, 更多的SO42-会强烈吸附在碳酸盐岩表面, 进一步降低岩石表面电势, 从而有利于Ca2+在碳酸盐岩表面的吸附。
Mg2+、SO42-作为改性剂改变碳酸盐岩表面润湿性的机理与Ca2+、SO42-一样(见图5b), 反应方程式为:
RCOO-— Ca— CaCO3(s)+Mg2++SO42-==
RCOO-— Ca++Mg— CaCO3(s) +SO42-
在砂岩油藏和碳酸盐岩油藏开发中均存在多组分离子交换机理, 但两类油藏中离子交换机理存在明显差异, 碳酸盐岩储集层适合用高矿化度海水驱, 而砂岩储集层适合用低矿化度水驱。
3.2.4 盐溶或盐析效应
极性有机物在水中的溶解度受水溶液中离子组分和浓度影响。有机物质溶解在水中时, 疏水部分周围会出现一层由氢键连接而成的水分子笼状结构, 有机组分即分布在这种结构中。无机离子(Ca2+、Mg2+、Na+)会破坏有机分子周围的水分子笼状结构, 因此降低了有机物质在水中的溶解度, 该过程称为盐析效应, 此时无机离子可以被称为水分子笼状结构破坏物[5]。阳离子破坏水分子笼状结构的能力与它们的水合作用强弱有关, 因此二价阳离子对有机物质在水中的溶解有更显著的影响。若注入水矿化度足够低(2 000~3 000 mg/L[47]), 将能有效增加有机物质在注入水中的溶解度, 该过程称为盐溶效应。盐溶效应能够溶解吸附在黏土矿物表面的有机物质, 从而改善矿物表面的亲水性, 因此盐溶效应也被认为是改进油藏亲水性和提高采收率的一种机理假设。Rezaeidoust等[5]研究发现随着注入水矿化度减小, 吸附在高岭石表面的4-叔丁基苯甲酸将会在水中再溶解或是从高岭石表面脱附下来。Hamam等[48]通过实验测试结果求得了一个盐析参数, 用来定量评价盐水矿化度对原油在盐水中溶解度的影响程度。
目前在研究油藏岩石表面润湿性控制机理时, 实验材料通常为天然岩心和原油, 润湿性评价方法主要为自渗吸实验。由于岩心表面矿物成分复杂, 原油也是一种复杂的多组分混合物, 所以如果对各组分不加区分来研究润湿性调节机理, 必将导致对该机理的理解存在片面性; 同时由于实验方法简单, 对岩石-盐水-原油之间的相互作用认识不清, 导致对机理的认识存在缺陷。因此在下一步的研究中, 应该将原油中界面活性组分分离, 然后针对不同矿物和原油组分进行实验研究, 实验中可采用多种辅助实验来验证盐水驱时控制岩石表面润湿性的微观机理, 对微观机理的正确认识有助于确定不同类型油藏盐水中离子组分, 从而建立一种有效利用盐水调节油藏润湿性的方法。
油藏岩石表面润湿性实质上是岩石表面、盐水和原油之间相互作用力的性质、大小、综合作用的宏观表现。岩石表面分布不同电量的基团, 它们依靠范德华力、氢键、库仑力和表面力与原油中有机物产生相互作用, 盐水的加入改变了岩石-盐水-原油间的受力平衡, 从而导致岩石表面润湿性发生改变。利用盐水调节岩石表面润湿性的机理包括:化学基团转化、界面电势改变、注入水pH值改变、多组分离子交换及盐溶/盐析效应。
通过合理设计注入水中的离子组成, 可有效调节岩石润湿性从而提高原油采收率。对砂岩油藏, 降低盐水中阳离子价态、盐水浓度或增加盐水pH值(对矿化度影响不大)有利于增强油藏岩石表面亲水性, 从而提高原油采收率; 对碳酸盐岩油藏, 高矿化度CaSO4、MgSO4盐水有利于增强油藏岩石表面亲水性, 从而利于进一步提高原油采收率。
符号注释:
A— — 岩石-原油-盐水体系中Hamaker常数, 约为10-20J[36]; As— — 系数, Pa; AH— — 有机酸; B— — 有机碱; A-, BH+— — 原油-盐水界面处有机酸、碱的解离产物; ci— — 注入水中离子i的浓度, mol/m3; e— — 单位电荷, C; E1— — 电荷与诱导偶极间的相互作用势能, J; E2— — 电荷和永久偶极间的相互作用势能, J; E3— — 电荷与电荷间的相互作用势能, J; [H+]∞ — — 砂岩表面定势离子H+在溶液体相中的浓度, mol/L; f-, f+— — 岩石表面中性基团(≡ T— OH)和正电性基团(≡ T— OH2+)的解离分数, 无因次; h— — 水膜厚度, m; hs— — 指数模型的特征衰减长度, m; i— — 离子; k— — Boltzmann常数, 1.381× 10-23 J/K; Kd-, Kd+— — 中性基团(≡ T— OH)和正电性基团(≡ T— OH2+)的解离常数, mol/L; NA— — Avogadro常数, mol-1; pc— — 毛管压力, Pa; Q1, Q2— — 岩石表面电量和原油中极性分子的带电量, C; r1— — 烃类化合物分子的中心与岩石表面基团中心的距离, m; r2— — 电荷与永久偶极间的距离, m; r3— — 两电荷中心间的距离, m; T— — 绝对温度, K; ≡ W— — 黏土矿物表面; z— — 离子的化合价; α — — 烃类化合物分子的极化率, C2· m2/J; ε — — 水溶液的相对介电常数, 无因次; ε 0— — 真空中的介电常数, 8.854× 10-12 F/m; θ — — 电荷与偶极矩的中心线和偶极矩轴方向之间的夹角, (° ); κ — — 双电层的厚度(即Debye长度)的倒数, m-1; μ — — 以氢键作用连接在岩石表面的有机基团的偶极矩, C· m; Π — — 分离压, Pa; σ 0— — 表面带电基团密度的最大值, C/m2; σ -, σ +— — 砂岩表面≡ T— O-、≡ T— OH2+密度, C/m2; φ 0— — 岩石表面电势, V; φ 1, φ 2— — 岩石-盐水界面、原油-盐水界面处的电势, V。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|